熱門資訊> 正文
3個月股價漲幅近一倍,中報首次盈利后亞盛醫藥-B(06855)估值增長再啟程
2024-08-23 09:20
今年上半年,港股醫藥板塊受外部因素影響出現較大幅度下跌。例如港股創新葯指數(931787)便在今年4月觸及歷史新低。而后雖有一定回彈,但年初至今該指數跌幅已達21.09%。
在此背景下,亞盛醫藥-B(06855)股價雖在今年Q1季度受大市影響出現一定回調,卻在4月中旬后走出了一條逆市大幅上漲的路徑。智通財經APP觀察到,在4月19日觸及階段性底部后,亞盛醫藥股價后續迅速拉昇,從低點15.42港元一路升至7月17日的高點30.10港元,區間累漲95.20%,接近翻倍。僅在6月,亞盛醫藥的單月股價累計漲幅便高達43.54%,創下了自2021年以來的月度股價漲幅新紀錄。
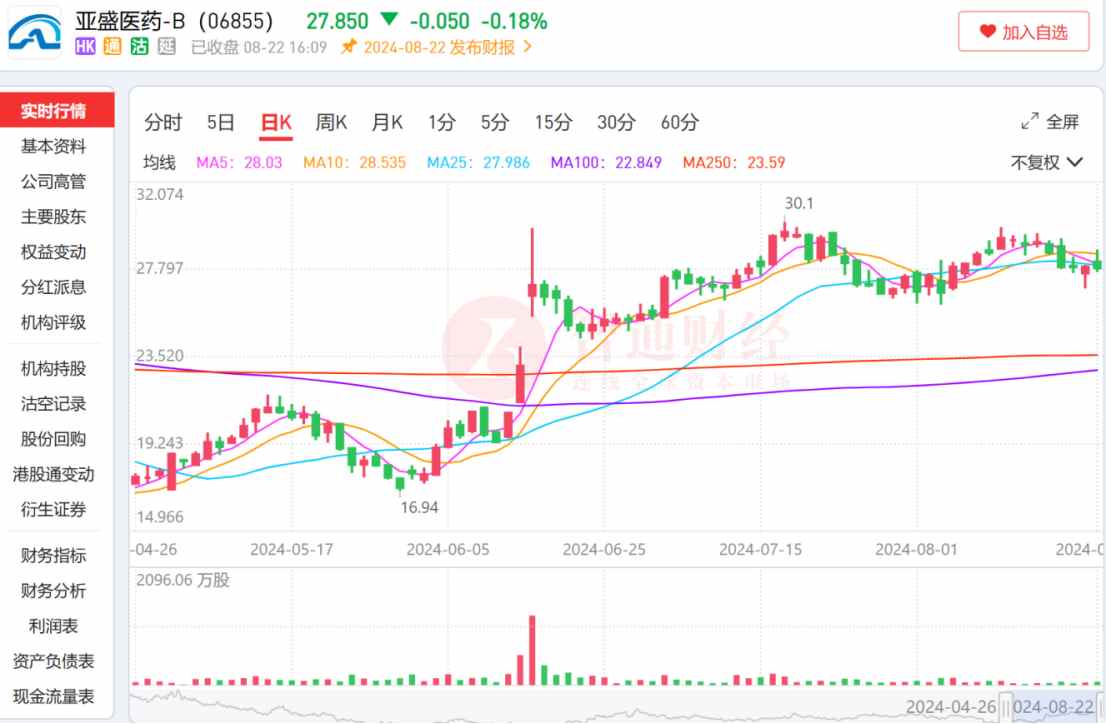
也就是説,在港股創新葯板塊波動未止的情況下,投資者選擇用腳投票助力亞盛醫藥股價實現率先反彈。而究其原因,則在於多重利好催化下,公司的「投資確定性」得到進一步驗證。
今年6月,亞盛醫藥與武田製藥就公司核心品種耐立克®簽署了一項總價達13億美元的具有「高首付、高里程碑、高分成」特點的獨家選擇權協議。同年7月,耐立克®在中國澳門獲批上市。此外,亞盛醫藥還宣佈即將赴美融資。
三箭齊發均指向當下港股創新葯投資邏輯的核心——現金流。
通過此次新鮮出爐的中期業績,投資者可以清晰看到,得益於重磅BD收入和耐立克®銷售,以及即將遞交新葯上市申請的APG-2575強勁的商業化預期,亞盛醫藥不僅實現了首次盈利,后續大幅淨現金狀態同樣可期,而持續抬高的股價也印證了亞盛醫藥作為一家俱備「投資確定性」的標杆藥企,自身內在價值正持續得到釋放。
持續挖掘核心品種全球商業化潛力
無論是今年2月耐立克®獲FDA批准治療經治CML-CP患者的全球註冊III期臨牀研究,還是6月公司宣佈與武田合作並宣佈即將赴美融資,,都體現了亞盛醫藥長期國際化戰略下的階段性成果。而其中的關鍵載體,便是商業化屢獲驗證的核心品種耐立克®。
從亞盛醫藥最新披露的2024年中報數據來看,報告期內,亞盛醫藥實現收入人民幣8.24億元,較去年同比大幅增長477%。與此同時,公司首次實現扭虧為盈,淨利潤達人民幣1.63億元。並且公司現金流持續獲得改善,保持穩健充沛。截至2024年7月初,貨幣資金余額為18億元。
報告期內,亞盛醫藥的商業化造血能力逐步增強。隨着商業化進度的快速推進,耐立克®當期實現銷售收入1.13億元,較去年下半年環比增長120%,較去年上半年同比增長5%。
從政策端來看,今年7月《全鏈條支持創新葯發展實施方案》獲審議通過。其中提到,針對創新葯的定價和支付問題,完善創新葯價格形成機制,制定鼓勵應用目錄,優先納入醫療機構用藥目錄,並建立醫保支付政策傾斜,增加創新葯使用規模。這無疑極大利好諸如耐立克®等真正具備重大創新性的藥物。
也就是説,隨着亞盛醫藥為耐立克®開闢更廣闊的適應症賽道,其后續的全球創新研發成果有望更高效轉化為公司的營收和利潤。
除此之外,公司與武田製藥的合作無疑今年上半年的「重頭戲」。雙方關於耐立克®(奧雷巴替尼)簽署的一項總價達13億美元的具有「高首付、高里程碑、高分成」特點的獨家選擇權協議,刷新了國內小分子腫瘤藥BD交易金額的新紀錄。武田製藥還投資7500萬美元,溢價25%認購公司股份,成為亞盛醫藥重要的產業股東。
值得一提的是,在簽署協議的一周內武田便完成7500萬美元股權認購,並在不到三周時間便支付了1億美元選擇權付款。武田積極合作的背后,側面反映出耐立克®巨大的全球商業化潛力。
據智通財經APP瞭解,去年11月,耐立克®獲批用於治療對一代和二代酪氨酸激酶抑制劑(TKI)耐藥和/或不耐受的慢性髓細胞白血病(CML)慢性期(-CP)成年患者。當時智通財經APP對此的判斷是:相較此前獲批的治療攜T315I突變耐藥CML的適應症,該適應症患者羣體規模更廣,能夠保證耐立克®后續銷售額持續增長。此次亞盛醫藥中報業績和耐立克®銷售業績的持續增長,也印證了耐立克®在擴大適應症範圍后的強勁實力。
亞盛醫藥也在依託自身強勁的全球創新能力,為耐立克®開闢更廣闊的適應症賽道。目前耐立克®對包括BCR-ABL、KIT、PDGFR、FGFR、b-RAF、DDR1、FLT3等多種激酶具有良好的活性,在多種血液腫瘤和實體瘤治療領域具有廣闊潛力。
在實體瘤領域,今年上半年,耐立克®在獲CDE納入突破性治療品種的基礎上,其治療SDH缺陷型GIST患者的III期臨牀研究再獲CDE許可。並且耐立克®在該領域的相關臨牀進展已連續兩年入選ASCO年會展示,在今年AACR年會上,耐立克®再次展現出在SDH缺陷型腫瘤適應症領域優異的抗腫瘤作用。
在血液瘤領域,耐立克®下一個增長點則來自費城染色體陽性(Ph+)急性淋巴細胞白血病(ALL)。
在此前一項針對既往接受過深度治療/難治性CML和Ph+ ALL患者的臨牀研究中,在普納替尼治療失敗的患者中,奧雷巴替尼治療組的CCyR率和MMR率分別為53%和38%;在阿思尼布治療失敗的患者中,奧雷巴替尼治療組的CCyR率和MMR率分別為43%和38%。這意味着耐立克®對三代BCR-ABL抑制劑競品耐藥或者無效的CML患者依然有效,且安全性大幅提升。
目前在Ph+ ALL適應症領域,耐立克®有望成為國內首個獲批用於一線治療Ph+ ALL的TKI藥物,市場確定性較強。參考相關適應症賽道的安進貝林妥歐單抗,其目前全球銷售爬坡已超10億美元。而在合作方武田的積極推動下,未來全球Ph+ ALL一線治療市場同樣有望為耐立克®帶來可觀的銷售增量。
全球創新閉環,夯實發展底座
亞盛醫藥之所以在今年上半年實現業績高速增長,耐立克®爆發強勁增長動能是主要原因,但其「研產銷」一體化創新閉環逐漸完善勢能積蓄同樣不容忽視。
財報顯示,今年上半年,亞盛醫藥確認研發投入達到4.44億元,強勁收入增長以及可觀的融資與現金流預期,為公司帶來的創新研發端的強支撐,夯實了公司探索全球差異化創新葯市場的基礎,推動公司加速向全球頭部Biopharma進發。
以亞盛醫藥細胞凋亡管線的核心品種Bcl-2抑制劑APG-2575為例,去年8月,APG-2575獲美國FDA批准開展用於治療既往接受治療的CLL/SLL患者的全球註冊性III期臨牀研究。這是繼該品種於2021年12月獲CDE批准開展用於治療R/R CLL/SLL患者的關鍵註冊II期臨牀研究后的又一重要里程碑。
此前多項臨牀數據也驗證其在全球血液腫瘤領域具有「同類最佳」(Best-in-class)潛力。這意味着APG-2575有望加速成為全球層面第二個獲批上市的Bcl-2抑制劑,躋身國際競爭陣營。
獲批全球註冊III期臨牀,也意味着APG-2575離國際市場商業化時間節點越來越近。以目前全球唯一一款獲批上市的Bcl-2抑制劑Venetoclax為例,其2022年銷售額達20.1億美元,同比增長10.4%。由於APG-2575與Venetoclax相較,安全性優勢更加突出且BIC潛力更大,因此市場預計APG-2575銷售峰值也有望超20億美元。
值得一提的是,APG-2575有望今年在國內遞交NDA,上市在即。憑藉其潛在的巨大商業化價值,APG-2575順利上市落地將是亞盛醫藥實現最終盈利的關鍵一環。
另外,在政策端的全鏈條支持下,亞盛醫藥也將成為最大的受益藥企之一。公司一直致力於原始創新和全球創新,目前正在中國、美國、澳大利亞、歐洲及加拿大開展40多項臨牀試驗。
管線方面,亞盛醫藥除了擁有奧雷巴替尼和APG-2575兩款具備十億美元分子潛力的核心產品外,還有諸如APG-115、APG-2449、APG-5918潛在的FIC/BIC在研產品,且其相關臨牀進展均在多個國際權威學術會議及期刊上公佈。此外,公司還通過在全球的520項授權專利,以及其中的367項海外授權專利構築了強大的全球知識產權佈局。
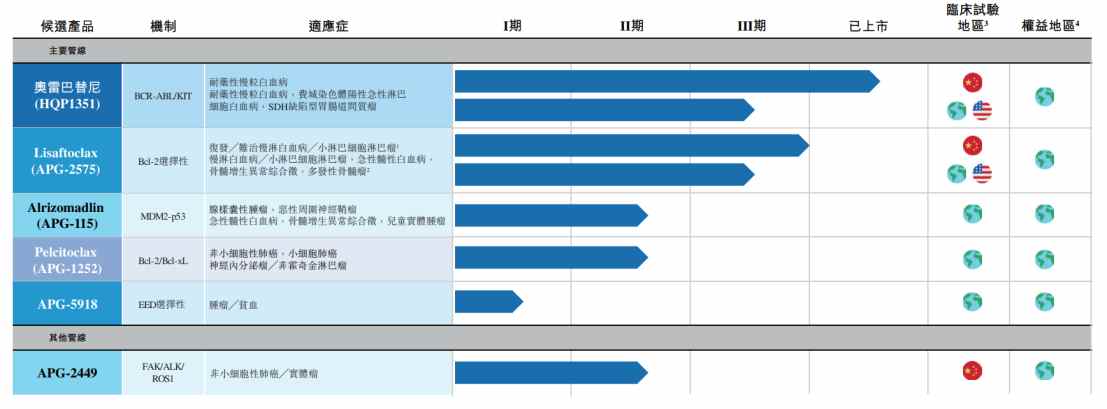
實際上無論是已實現商業化的耐立克®或是即將上市的APG-2575,還是細胞凋亡管線中的眾多FIC/BIC產品,亞盛醫藥所展現出的成熟管線進度正符合當下全球生物醫藥投資的偏好。
數據顯示,今年6月,美國及歐洲的生物醫藥行業共發生32起融資事件,融資規模達23.2億美元,融資規模重回加息前水平。另據摩根大通數據,今年上半年,美國生物製藥行業的風投活動顯示出復甦跡象,第二季度尤其活躍。且第二季度的投資主要集中在最有前景的治療領域和后期項目上,臨牀階段的生物製藥公司獲得了更高的中位數投資輪次。
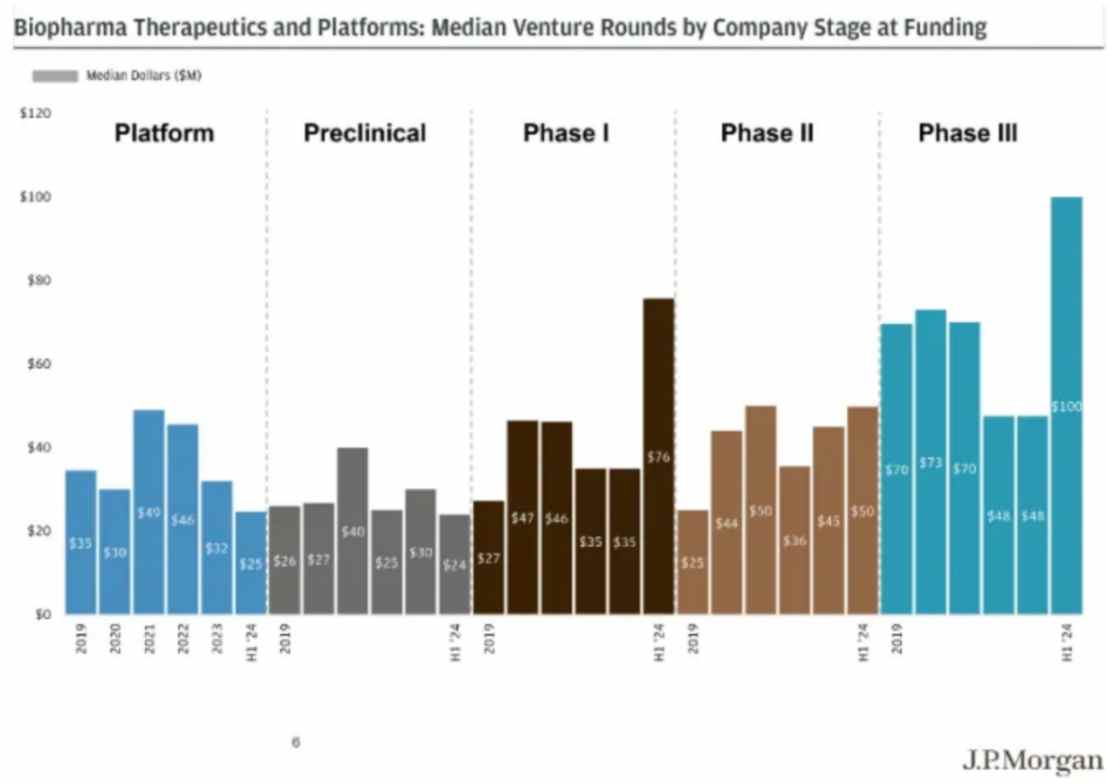
也就是説,目前美股生物醫藥投資中,投資者偏好「更具確定性的企業」,而手握多項具備重磅FIC/BIC潛力后期資產的亞盛醫藥,無疑將成為美股市場稀缺的高價值生物醫藥投資標的。
結語
目前,美聯儲9月降息預期確定性逐漸提高,全球生物醫藥融資「全面解凍」在望。在行業即將復甦的關鍵時間窗口,亞盛醫藥拿出了一份關鍵管線研發與全球商業化進程的同步快速順利推進的亮眼財報,值得港美股投資者保持高度關注。
未來在充沛現金流支撐下,亞盛醫藥有望憑藉不斷完善的研產銷創新閉環,在全球化研發、海外註冊以及國際商業化等多領域體系化競爭中向國際頭部Biopharma加速躍遷,不斷釋放自身的內在價值。
推薦文章
美股機會日報 | 就業數據轉弱!美國至2月7日當周初請失業金人數超預期;存儲概念股盤前齊升,閃迪大漲超7%
要點速遞!《跑贏美股》春節特別直播核心觀點總結
華盛早報 | 非農數據大超預期!首次降息或延至7月;AI恐慌交易蔓延至房地產服務板塊, CBRE暴跌12%;智譜發佈新模型
美股機會日報 | 經濟數據強勁!美國1月非農就業大超預期,納指期貨漲至0.6%;AI應用股業績超預期,Shopify漲超10%
資金覆盤 | 北水淨買入港股超48億港元,逾7億港元搶籌騰訊
華盛早報 | 「AI威脅」波及華爾街!財富管理公司全線暴跌;豆包官宣「參戰」!春節AI紅包戰愈演愈烈
美股機會日報 | 科技巨頭迎利好?特朗普政府擬結構性豁免芯片關税;臺積電1月銷售額創歷史新高,盤前股價漲近3%
一圖看懂 | 淨利大增60.7%!中芯國際Q4營收24.9億美元,同比增長12.8%

